Teoria e terminologia introduttive
La risonanza magnetica nucleare (NMR) è una tecnica usata per analizzare la struttura di molte molecole chimiche, primariamente composti organici. Un composto tipico si compone ad esempio di atomi di carbonio, idrogeno e ossigeno.
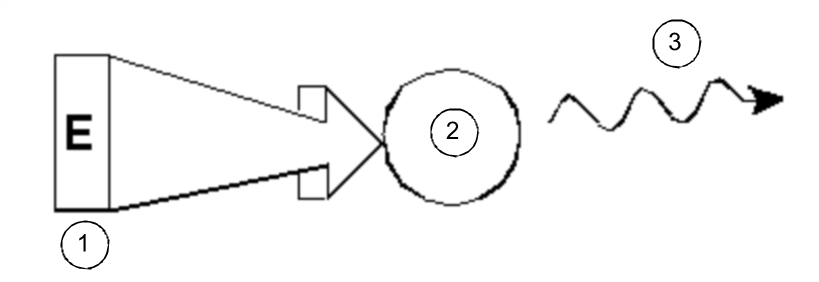
Nella sua forma più semplice, un esperimento NMR si compone di tre fasi:
- 1.
- Collocazione del campione in un campo magnetico statico.
- 2.
- Eccitazione dei nuclei del campione mediante impulso di radiofrequenza.
- 3.
- Misurazione della frequenza dei segnali emessi dal campione.
Eccitazione e risposta
Dalle frequenze emesse, gli analisti possono trarre informazioni relative al legame e alla disposizione degli atomi nel campione. I nuclei NMR attivi del campione risuonano a frequenze diverse, denominate "frequenze di risonanza“. Si tratta delle frequenze emesse dai nuclei sottoposti ad eccitazione dagli impulsi di radiofrequenza in ingresso. Il valore della frequenza di risonanza dipende da due fattori:
1) Tipo di nucleo:
Ogni isotopo ha una particolare combinazione di protoni e neutroni nel proprio nucleo. La struttura del nucleo determina in larga misura il valore della frequenza di risonanza. Pertanto, ciascun isotopo rivela una “frequenza di risonanza di base”. I nuclei 13C avranno una frequenza di risonanza di base diversa rispetto ai nuclei di 1H, ecc. Si osservi la grande variazione delle frequenze di risonanza di base dei diversi isotopi elencati nella tabella seguente:
Tabella dei dati di vari isotopi (le frequenze citate si riferiscono ad un magnete 11.7T)
2) Ambiente atomico locale
Alla frequenza di risonanza di base si sovrappone un effetto dovuto all'ambiente atomico locale in cui è situato l'isotopo. Il valore preciso della frequenza di risonanza di un nucleo 1H in un determinato composto, dipenderà dagli atomi ai quali è legato e dai quali è circondato. Il nucleo è circondato da elettroni, i quali possono essere considerati cariche elettriche in movimento, con campi magnetici associati. Questi elettroni fungono da fonte di schermatura magnetica per il nucleo. L'entità della schermatura dipenderà dall'ambiente atomico locale specifico. Le dimensioni delle variazioni del campo locale tipico (risultanti in una variazione di frequenza) dipenderanno dall'isotopo e dalla forza del campo magnetico in cui si trova il campione. Nella tabella sottostante è indicata la variazione di frequenza tipica dei nuclei NMR maggiormente usati: 1H e 13C. È chiaro che l'ambiente atomico locale ha un effetto relativamente piccolo sulla frequenza di risonanza di base.
Variazioni di frequenza (riferite ad un magnete 11,7 T)
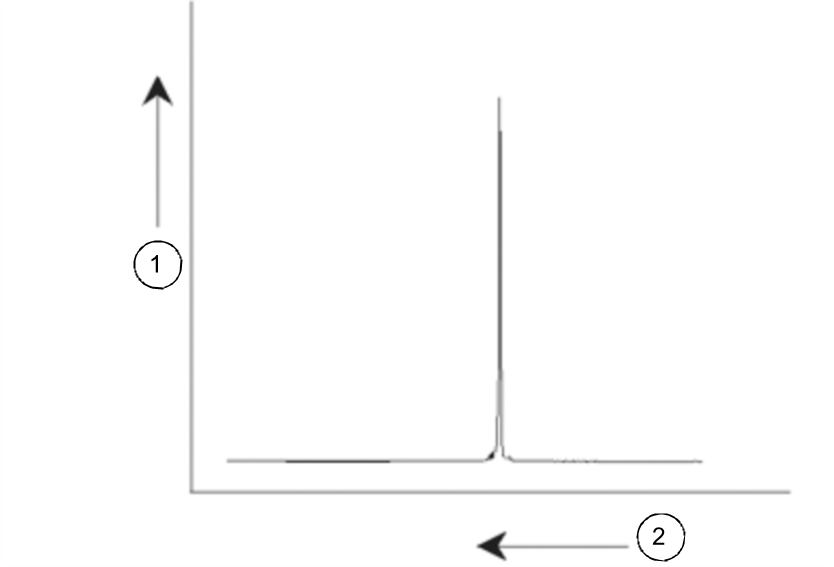
I segnali NMR vengono normalmente tracciati come spettri e analizzati in base a due caratteristiche: la frequenza e l'intensità. Convenzionalmente, in NMR la frequenza viene tracciata su un asse orizzontale, segnandone l'aumento verso sinistra.
Spettro NMR
Come spiegato nei paragrafi precedenti, la frequenza fornisce informazioni qualitative in merito all'ambiente atomico locale. L'intensità integrata di un segnale è la misura indicante la potenza del segnale e si determina integrando l'area sottostante il picco del segnale. L'integrazione sarà direttamente proporzionale al numero di nuclei che contribuiscono ad un segnale ad una determinata frequenza (a condizione che i nuclei siano sottoposti alla stessa eccitazione) e fornirà quindi un'informazione quantitativa in merito alla struttura chimica.
Per eccitare un certo nucleo in un esperimento NMR, la frequenza dell'impulso di eccitazione dovrebbe corrispondere strettamente alla frequenza di risonanza del nucleo. Questa frequenza viene indicata come frequenza portante. Pertanto, se si svolgono esperimenti utilizzando un magnete 11,7 T, i nuclei 1H richiederebbero una frequenza portante di circa 500 MHz, mentre i nuclei 13C richiederebbero una frequenza portante prossima ai 126 MHz. La frequenza portante viene indicata dal parametro SFO1. Il nucleo eccitato da questa frequenza portante viene indicato come nucleo di osservazione.
Si osservi che ci sono esperimenti in cui viene sottoposto ad eccitazione più di un nucleo, es. durante il trasferimento di polarizzazione o il disaccoppiamento. In questi casi si ha più di una frequenza portante, ma pur sempre una sola frequenza di osservazione.
Non tutti gli isotopi rispondono agli impulsi di radiofrequenza, il che significa che non tutti sono NMR attivi. In natura esistono tre isotopi dell'elemento idrogeno: 1H (idrogeno), 2H (deuterio), e 3H (trizio, radioattivo!). La presenza in natura di questi isotopi è rispettivamente di 99,98%, 0,015% e 0,005%. Tutti e tre sono NMR attivi, anche se, come mostra la tabella 3.1, essi rivelano una grande variazione di frequenza di risonanza. Per analizzare un campione di idrogeno, viene sottoposto ad eccitazione l'isotopo 1H, in quanto si tratta del tipo di isotopo più abbondante in assoluto. Degli isotopi di carbonio presenti in natura, solo uno è NMR attivo. L'isotopo più comune in assoluto, 12C (abbondanza in natura pari al 98,89%) è inattivo. Pertanto, l'analisi NMR dei campioni organici, per quanto concerne il carbonio, dipende dai segnali emessi dall'isotopo 13C , presente in natura solo per l'1,11%. Ovviamente, l'analisi NMR del carbonio è più difficile rispetto, ad esempio, a quella di 1H (ci sono poi altri fattori riguardanti la sensibilità che verranno trattati nelle prossime sezioni di questo capitolo).
In base alla breve introduzione precedente sulla risonanza magnetica nucleare, è un buon esercizio considerare come applicare questa tecnica per analizzare la composizione del cloroformio (CHCl3).
Ulteriori informazioni