Introducción a la Teoría y Terminología
La RMN es una técnica utilizada para analizar la estructura de muchas moléculas químicas, principalmente compuestos orgánicos. Un compuesto típico estaría formado por átomos de carbono, hidrógeno y oxígeno.
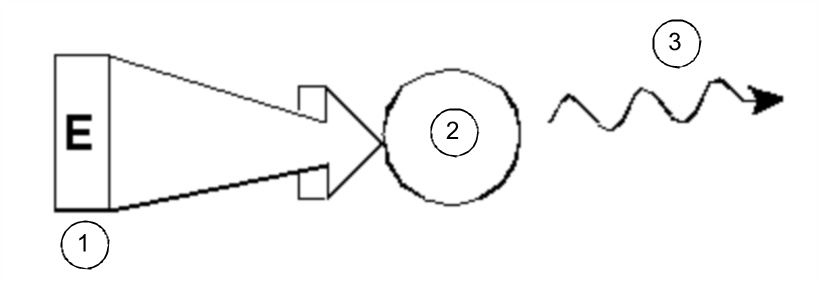
La forma más simple de un experimento de RMN consta de tres etapas:
- 1.
- Colocar la muestra en un campo magnético estático.
- 2.
- Excitar los núcleos de la muestra con un pulso de radiofrecuencia.
- 3.
- Medir la frecuencia de las señales emitidas por la muestra.
Excitación y respuesta
A partir de las frecuencias emitidas, los analistas pueden deducir información acerca de los enlaces y la disposición de los átomos en la muestra. Los núcleos activos en RMN de la muestra resuenan a diferentes frecuencias llamadas “frecuencias de resonancia”. Estas son las frecuencias emitidas por los núcleos cuando son excitados por el pulso de radiofrecuencia entrante. El valor de una frecuencia de resonancia depende de dos factores:
1) Tipo de núcleo:
Cada isótopo tiene una combinación particular de protones y neutrones en su núcleo. La estructura nuclear determina, en gran parte, el valor de la frecuencia de resonancia. Así cada isótopo muestra una “frecuencia de resonancia básica”. El núcleo de 13C tendrá una frecuencia de resonancia básica diferente en comparación con la del núcleo 1H etc. Observe la gran variación entre las frecuencias de resonancia básicas de los distintos isótopos según se muestran en la siguiente tabla:
Tabla de datos para varios isótopos (frecuencias expresadas para un imán de 11.7T)
2) Entorno atómico local:
A la frecuencia de resonancia básica se le suma el efecto provocado por el entorno atómico local en él que el isótopo está situado. El valor exacto de la frecuencia de resonancia de un núcleo de 1H en un compuesto determinado dependerá de los átomos a los que esté enlazado y de los que esté rodeado. El núcleo está rodeado de electrones, que se pueden representar como cargas eléctricas en movimiento con campos magnéticos asociados. Estos electrones actúan como fuente de apantallamiento magnético para los núcleos. La magnitud del apantallamiento dependerá del entorno atómico local exacto. La magnitud de las variaciones del campo local normal (que darán como resultado una variación de frecuencia emitida) dependerán del isótopo y de la intensidad del campo magnético en él que se sitúa la muestra. La tabla siguiente muestra las variaciones de frecuencias típicas para los dos núcleos más comúnmente utilizados en RMN, 1H y 13C. Es evidente que el entorno atómico local tiene un efecto relativamente pequeño sobre la frecuencia de resonancia básica.
Variaciones de frecuencia (para un imán de 11.7 T)
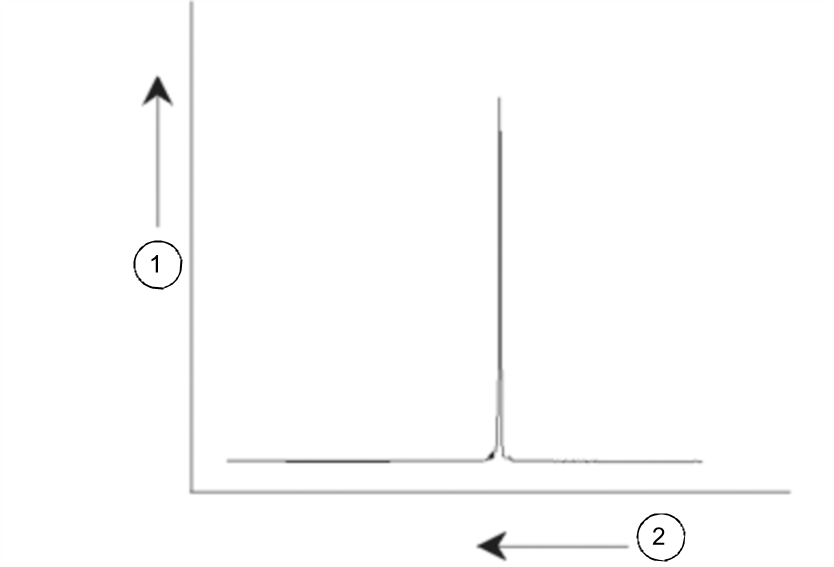
Las señales de RMN habitualmente se representan en forma de espectros y se analizan en relación a dos características, frecuencia e intensidad. Convencionalmente en RMN la frecuencia se representa en el eje horizontal, y aumenta hacia la izquierda.
Espectro de RMN
Tal como se ha mencionado, la frecuencia proporciona información cualitativa respecto al entorno atómico local. La intensidad integrada de una señal es una medida de la intensidad de la señal y se determina integrando el área bajo el pico de la señal. La integral será directamente proporcional al número de núcleos que contribuyan a esa señal a una frecuencia particular (si todos los núcleos son excitados de la misma forma) y por tanto proporcionará información cuantitativa sobre la estructura química.
Para excitar un determinado núcleo en un experimento de RMN, la frecuencia del pulso de excitación debe ser muy parecida a la frecuencia de resonancia del núcleo. Esta frecuencia se denomina frecuencia portadora (carrier frequency). Así, si el experimento se lleva acabo en un imán de 11.7 T, el núcleo de 1H requerirá una frecuencia portadora de aproximadamente 500 MHz, mientras que el núcleo de 13C necesitará una frecuencia portadora cercana a 126 MHz. La frecuencia de transmisión se especifica con el parámetro SFO1. El núcleo que se excita por esta frecuencia portadora se denomina núcleo observado.
Tenga en cuenta que hay experimentos donde se excita a más de un núcleo, por ejemplo, durante la transferencia de polarización o el desacoplamiento. En estos casos hay más de una frecuencia portadora, sin embargo sólo una frecuencia observada.
No todos los isótopos responderán a pulsos de radiofrecuencia, o sea no todos son activos en RMN. En la naturaleza se pueden encontrar tres isótopos del hidrógeno: 1H (hidrógeno), 2H (deuterio), y 3H (tritio, ¡radioactivo!). La abundancia natural de estos isótopos es de 99.98%, 0.015%, y 0.005% respectivamente. Los tres núcleos son activos en RMN, si bien, según se puede ver en la tabla 3.1, muestran una gran variación entre sus frecuencias de resonancia. Para analizar el espectro de hidrógeno de una muestra, se excita el 1H, que es el isótopo más abundante de lejos. De los isótopos del carbono que se encuentran en la naturaleza, sólo uno es activo en RMN. El isótopo más común, 12C (abundancia natural 98.89%), es inactivo. Por tanto, el análisis de RMN de carbono de compuestos orgánicos se basa en las señales emitidas por el isótopo 13C, que tiene una abundancia natural de solo un 1.11%. Obviamente, el análisis de RMN para el carbono es más difícil que para, por ejemplo, el 1H. (Existen otros factores que afectan a la sensibilidad. Estos se discutirán en la siguiente sección de este capítulo).
Un buen ejercicio para aplicar esta breve introducción a la RMN, podría ser ver como está técnica se podría aplicar para determinar la composición del cloroformo (CHCl3).
Informacion adicional