Introduction à la théorie et à la terminologie
La résonance magnétique nucléaire (RMN) est une technique destinée à l'analyse structurale des molécules, et principalement des molécules organiques. Un composé typique peut être constitué, par exemple, d'atomes de carbone, d'hydrogène et d'oxygène.
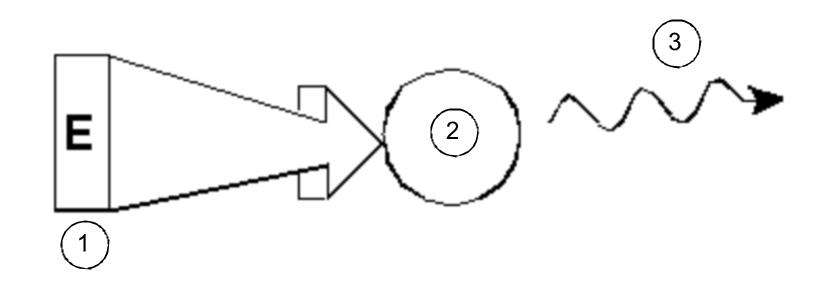
Dans sa forme la plus simple, une expérience RMN comprend trois étapes :
- 1.
- introduction de l'échantillon dans un champ magnétique statique ;
- 2.
- excitation des noyaux de l'échantillon par une impulsion de radiofréquence (RF) ;
- 3.
- mesure de la fréquence du courant induit par l'échantillon lors de la relaxation des noyaux.
Excitation et réponse
Les spectroscopistes sont en mesure de déduire des informations relatives aux liaisons et à la disposition des atomes dans la molécule à partir des fréquences mesurées. Les noyaux actifs en RMN présents dans l'échantillon résonnent à différentes fréquences, appelées « fréquences de résonance ». Il s'agit des fréquences absorbées par les noyaux quand ils sont excités par l'impulsion de radiofréquence. La valeur d'une fréquence de résonance dépend de deux facteurs :
1) la nature isotopique du noyau :
Chaque isotope est composé de protons et de neutrons. La structure du noyau détermine, dans une large mesure, la valeur de la fréquence de résonance. Chaque isotope possède ainsi une « fréquence de résonance de base ». La fréquence de résonance de base des noyaux 13C est donc différente de celle des noyaux 1H, etc. Le tableau suivant répertorie les valeurs des fréquences de résonance de base - arrondies au MHz - de différents isotopes, offrant ainsi un aperçu de l'importance de ces variations :
Tableau des données des différents isotopes (fréquences indiquées pour un aimant de 11.7T)
2) Environnement chimique local :
Outre la fréquence de résonance de base, il faut également tenir compte de l'effet résultant de l'environnement chimique local dans lequel se trouve un isotope. La valeur précise de la fréquence de résonance d'un noyau 1H dans un composé particulier dépendra des atomes auquel il est lié et aussi de ceux qui l'entourent. Le noyau est entouré d'électrons qui peuvent être considérés comme des charges électriques en mouvement avec des champs magnétiques associés. Ces électrons font office de source de blindage magnétique pour le noyau. L'étendue du blindage dépendra de l'environnement chimique local précis. L'importance des variations du champ local (qui entraînent une variation de la fréquence) dépendra de l'isotope et de l'intensité du champ magnétique dans lequel l'échantillon est placé. Le tableau ci-dessous indique la variation de fréquence typique pour les deux noyaux les plus utilisés en RMN, 1H et 13C. Il est évident que l'environnement chimique local a un faible impact sur la fréquence de résonance de base.
Variations de fréquence (indiquées pour un aimant 11.7 T)
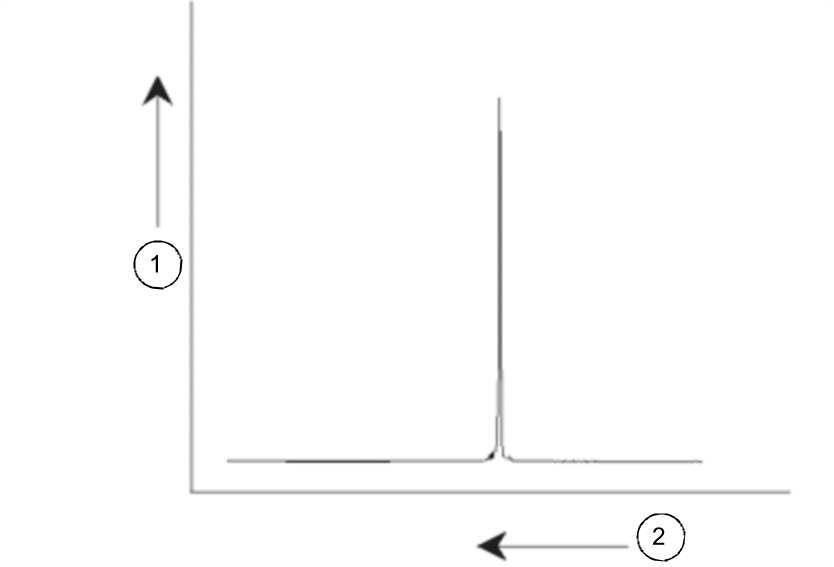
Les signaux de RMN sont généralement représentés sous forme de spectre, leur analyse reposant sur les deux facteurs que sont la fréquence et l'intensité. En RMN, la variation de la fréquence est représentée selon l'axe horizontal, en augmentant de la droite vers la gauche.
Spectre RMN
Comme indiqué précédemment, la fréquence fournit des informations qualitatives quant à l'environnement chimique local. L'intégrale (surface) d'un pic est une mesure de l'intensité du signal. Elle est déterminée par l'intégration de la zone située sous le pic. L'intégrale est directement proportionnelle au nombre de noyaux contribuant à un signal de fréquence donnée (si les noyaux sont tous également excités) et fournira, par conséquent, des informations quantitatives sur la structure moléculaire.
Pour exciter un noyau donné dans le cadre d'une expérience RMN, la fréquence de l'impulsion d'excitation doit correspondre à la fréquence de résonance du noyau. Cette fréquence est appelée la fréquence porteuse. Donc, si les expériences sont exécutées avec un aimant 11.7 T, les noyaux 1H requièrent une fréquence porteuse d'env. 500 MHz, tandis que les noyaux 13C requièrent une fréquence porteuse proche de 126 MHz. La fréquence porteuse est définie par le paramètre SFO1. Le noyau excité par cette fréquence porteuse est le noyau observé.
Il est à noter qu'il existe des expériences dans lesquelles plus d'un noyau est excité, par ex. lors du transfert de polarisation ou du découplage. Dans ce cas, il y a plus d'une fréquence porteuse, mais une seule fréquence d'observation.
Les isotopes ne répondent pas tous aux impulsions de radiofréquence, ils ne sont donc pas tous actifs en RMN. L'élément hydrogène possède trois isotopes que l'on trouve dans la nature : 1H (hydrogène), 2H (deutérium), et 3H (tritium, radioactif !). L’abondance isotopique naturelle des deux premiers est de 99,985 % et 0,015 %, le troisième est présent à l'état de traces. Ils sont tous les trois actifs en RMN, bien qu'ils présentent une variation importante de fréquence de résonance, comme le montre le tableau 3.1. Dans le cadre de l'analyse d'un échantillon pour l'hydrogène, c'est l'isotope 1H qui est observé puisque cet isotope est de loin le plus abondant. Parmi les isotopes du carbone se trouvant dans la nature, seul un isotope est actif en RMN : l'isotope le plus courant, 12C (abondance isotopique naturelle de 98,89 %) est inactif. Par conséquent, l'analyse par RMN des composés organiques pour le carbone repose sur les signaux provenant de l'isotope 13C dont l’abondance isotopique naturelle est de 1,11 % seulement. De toute évidence, l'analyse par RMN pour le carbone est plus difficile que celle de 1H par exemple (d'autres facteurs affectent la sensibilité, ceux-ci seront traités ultérieurement dans le présent chapitre).
En se basant sur la brève introduction au principe de la RMN présentée ci-dessus, nous allons réfléchir à la façon dont cette technique pourrait être utilisée pour analyser la composition du chloroforme (CHCl3), ce qui constituera un bon exercice.
Les informations supplementaires